Cuando eliges un péptido, el parámetro más importante que determina su calidad no es el precio, el envase ni la marca del proveedor. Es un número: la pureza porcentual determinada mediante HPLC. Este valor — aparentemente sencillo — es el resultado de un análisis sofisticado que revela con precisión qué contiene realmente el vial que tienes entre manos.
Piensa en péptidos como la retatrutida — que en nuestro blog llamamos TRIPLE-G por sus tres G (GLP-1, GIP, Glucagón): es una molécula compleja, con 39 aminoácidos. Cada paso de su síntesis puede introducir impurezas. Por eso la pureza es tan importante.
En este artículo profundizamos en todo lo que necesitas saber sobre el HPLC aplicado a péptidos: cómo funciona, cómo interpretar los resultados, por qué la diferencia entre 95% y 99%+ no es trivial y cómo verificar las declaraciones de pureza de los proveedores.
Qué es el HPLC
Definición y Principio
El HPLC (High-Performance Liquid Chromatography, o cromatografía líquida de alto rendimiento) es una técnica analítica que separa, identifica y cuantifica los componentes de una mezcla líquida. En palabras simples, es la mejor herramienta que tenemos para medir cuán puro es un péptido. Es el estándar de oro en todo el mundo.
El principio fundamental es sencillo: una mezcla de compuestos se arrastra a través de una columna cromatográfica mediante un disolvente (la llamada “fase móvil”). Los diferentes componentes de la mezcla interactúan de forma distinta con el material de relleno de la columna (la “fase estacionaria”) y se separan según sus propiedades fisicoquímicas. Los componentes que interactúan débilmente con la fase estacionaria eluyen (es decir, salen de la columna) primero; los que interactúan más fuertemente eluyen después.
Componentes de un Sistema HPLC
Un sistema HPLC típico comprende:
- Depósito de disolvente: contiene la fase móvil (mezclas de agua/acetonitrilo con ácido trifluoroacético son las más comunes para péptidos)
- Bomba de alta presión: impulsa la fase móvil a través de la columna a presiones de 50-400 bar
- Inyector: introduce la muestra (el péptido a analizar) en el flujo de disolvente
- Columna cromatográfica: el corazón del sistema, típicamente una columna C18 de fase inversa de 100-250 mm de longitud con diámetro interno de 4,6 mm
- Detector UV: mide la absorbancia de luz ultravioleta de los compuestos que eluyen de la columna (los péptidos absorben típicamente a 214 nm o 220 nm)
- Sistema de adquisición de datos: software que genera el cromatograma
HPLC de Fase Inversa (RP-HPLC) para Péptidos
Para el análisis de péptidos, la modalidad más utilizada es la fase inversa (Reversed-Phase, RP-HPLC). En esta configuración:
- La fase estacionaria es apolar (cadenas C18 unidas a sílice)
- La fase móvil es polar (gradiente agua a acetonitrilo)
Los péptidos, que poseen regiones tanto polares como apolares, se separan en función de su hidrofobicidad: los péptidos más hidrofílicos eluyen primero, los más hidrofóbicos después. Esta técnica es excelente para separar el péptido objetivo de las impurezas de síntesis, que a menudo difieren en uno o pocos aminoácidos.
Cómo Leer un Cromatograma
El Resultado del Análisis
El resultado de un análisis HPLC es un cromatograma: un gráfico con el tiempo de retención (minutos) en el eje X y la intensidad de la señal UV (miliabsorbancia, mAU) en el eje Y.
Elementos Clave del Cromatograma
El pico principal (Main Peak): es el pico más alto y prominente del cromatograma, correspondiente al péptido objetivo. Su posición en el eje X es el tiempo de retención — un valor característico que depende de la estructura del péptido y de las condiciones analíticas. Para un método HPLC dado, el tiempo de retención es reproducible y permite la identificación del compuesto.
Los picos de impureza: son los picos más pequeños que aparecen antes, después o a los lados del pico principal. Cada pico corresponde a una impureza diferente — un péptido truncado, una forma oxidada, un isómero o un subproducto de la síntesis.
La línea base: es la línea horizontal del cromatograma en ausencia de compuestos que eluyen. Una línea base estable y plana indica un análisis bien realizado.
El área del pico: la pureza se calcula como:
Pureza (%) = (Área del pico principal / Área total de todos los picos) x 100
Por ejemplo, si el pico principal tiene un área de 990 unidades y el área total de todos los picos es de 1000 unidades, la pureza es del 99,0%.
Cómo Evaluar un Cromatograma de Calidad
Un buen cromatograma presenta:
- Pico principal simétrico: un pico asimétrico (con “cola” o “frente”) puede indicar problemas cromatográficos o una mezcla de isómeros
- Línea base plana: oscilaciones en la línea base sugieren problemas instrumentales o contaminación de los disolventes
- Buena resolución: los picos de impureza deben estar claramente separados del pico principal
- Escala temporal adecuada: el gradiente debe ser suficientemente largo para separar los componentes
El Sistema de Clasificación de la Pureza
No todos los péptidos son iguales. La industria utiliza un sistema de clasificación basado en la pureza HPLC:
Grados de Pureza
| Grado | Pureza HPLC | Uso típico | Coste relativo |
|---|---|---|---|
| Crudo (crude) | <70% | No apto para investigación | Muy bajo |
| Research grade | mayor de 95% | Screening inicial, estudios preliminares | Bajo |
| High purity | mayor de 98% | Investigación estándar, la mayoría de los estudios | Medio |
| Premium | mayor de 99% | Estudios cuantitativos precisos, in vivo | Alto |
| Ultra-premium | mayor de 99,5% | Estudios de referencia, dosis-respuesta críticos | Muy alto |
Qué Significan en la Práctica
La diferencia numérica entre 95% y 99% puede parecer modesta — solo 4 puntos porcentuales. Pero veamos qué significa en términos de contenido efectivo:
Péptido al 95% de pureza: de 10 mg de polvo, 9,5 mg son el péptido deseado y 0,5 mg son impurezas. Si preparas una solución a 5 mg/ml, cada mililitro contiene 0,25 mg de impurezas desconocidas.
Péptido al 99% de pureza: de 10 mg de polvo, 9,9 mg son el péptido deseado y solo 0,1 mg son impurezas — cinco veces menos que al 95%.
Péptido al 99,5% de pureza: de 10 mg de polvo, 9,95 mg son el péptido deseado y apenas 0,05 mg son impurezas — diez veces menos que al 95%.
Péptido al 99,8% de pureza: de 10 mg de polvo, 9,98 mg son el péptido deseado y solo 0,02 mg son impurezas — veinticinco veces menos que al 95%.
Por Qué la Pureza Importa: las Razones Científicas
Los péptidos como el GLP-1 son mensajeros biológicos que tu cuerpo ya produce de forma natural — por ejemplo, el GLP-1 se libera después de cada comida para señalar la saciedad. Cuando usas una versión sintética como la semaglutida o el TRIPLE-G, quieres que sea lo más idéntica posible a la señal natural, sin “ruido” químico.
1. Reproducibilidad de los Resultados
El principio fundamental de la ciencia es la reproducibilidad: un experimento realizado en las mismas condiciones debe producir los mismos resultados. Las impurezas introducen variabilidad en los resultados porque:
- La composición y concentración de las impurezas varían de lote a lote
- Algunas impurezas pueden tener actividad biológica propia (agonista o antagonista)
- El “ruido” de las impurezas oscurece la señal del péptido objetivo
Con un péptido al 99,5%+, la variabilidad introducida por las impurezas es despreciable y los resultados son altamente reproducibles.
2. Precisión de la Dosificación
En cualquier estudio dosis-respuesta, la precisión de la dosificación es crítica. Si el péptido tiene una pureza del 95%, cada dosis nominal contiene efectivamente un 5% menos de principio activo respecto a lo calculado. Para estudios que miden diferencias finas entre dosificaciones (por ejemplo, 100 mcg vs. 250 mcg vs. 500 mcg), esta imprecisión puede:
- Desplazar la curva dosis-respuesta
- Alterar la determinación del EC50
- Producir datos irreproducibles entre laboratorios que usan péptidos de distinta pureza
3. Reducción de Efectos Confundentes
Las impurezas no son inertes. En un contexto de investigación, pueden:
- Generar falsos positivos: una impureza con actividad biológica propia puede producir un efecto atribuido erróneamente al péptido objetivo
- Causar toxicidad: subproductos de la síntesis (agentes de acoplamiento residuales, disolventes) pueden ser citotóxicos
- Interferir con los ensayos: impurezas fluorescentes o con absorción UV pueden interferir con ensayos espectrofotométricos o inmunológicos
4. Menor Dosis Efectiva Necesaria
Un corolario práctico de la alta pureza es que se necesitan dosis nominales inferiores para obtener el mismo efecto biológico. Un péptido al 99,8% requiere aproximadamente un 5% menos de material que uno al 95% para obtener la misma concentración efectiva de principio activo. Esto puede traducirse en un ahorro significativo en estudios que requieren grandes cantidades de péptido.
Impurezas Comunes en la Síntesis Peptídica
Origen de las Impurezas
La síntesis peptídica en fase sólida (SPPS, Solid-Phase Peptide Synthesis) es un proceso químico complejo en el que se ensamblan aminoácidos uno a uno sobre un soporte sólido. Cada paso de acoplamiento (adición de un aminoácido) tiene una eficiencia inferior al 100%, generando impurezas características.
Tipos Principales de Impurezas
Péptidos de deleción (Deletion Peptides): se producen cuando un aminoácido no se incorpora a la secuencia. El resultado es un péptido al que le falta uno o más residuos. Para un péptido de 39 aminoácidos como el TRIPLE-G (retatrutida), la deleción de un solo residuo produce un péptido con peso molecular inferior en aproximadamente 100-200 Da.
Péptidos truncados (Truncated Peptides): la síntesis se interrumpe prematuramente, generando fragmentos de la secuencia objetivo. Son típicamente las impurezas principales en péptidos de baja pureza.
Formas oxidadas: la metionina y el triptófano pueden oxidarse durante la síntesis o la purificación. El sulfóxido de metionina es la impureza de oxidación más común.
Epímeros (D-aminoácidos): durante el acoplamiento, la racemización parcial puede convertir L-aminoácidos en D-aminoácidos, generando diastereómeros del péptido objetivo.
Péptidos con deamidación: la asparagina y la glutamina pueden sufrir deamidación (conversión en ácido aspártico y glutámico respectivamente), generando impurezas con carga diferente.
Residuos de agentes de acoplamiento y disolventes: trazas de HBTU, HATU, DMF, NMP u otros reactivos de la síntesis pueden copurificarse con el péptido.
Cuantificación de las Impurezas
Un informe HPLC completo identifica no solo la pureza total, sino también las impurezas individuales con su abundancia relativa. Un informe de alta calidad indica:
- Pureza del pico principal (%)
- Lista de impurezas detectables con su tiempo de retención y abundancia (%)
- Límite de detección del método
- Condiciones analíticas (columna, gradiente, detector)
Cómo Verificar las Declaraciones de Pureza
El Problema de la Autodeclaración
El mercado de péptidos para investigación presenta un problema estructural: muchos proveedores declaran purezas elevadas (99%+) sin aportar evidencia analítica verificable. Las declaraciones de pureza no respaldadas por datos son, en el mejor de los casos, poco fiables.
Certificado de Análisis (CoA) Interno
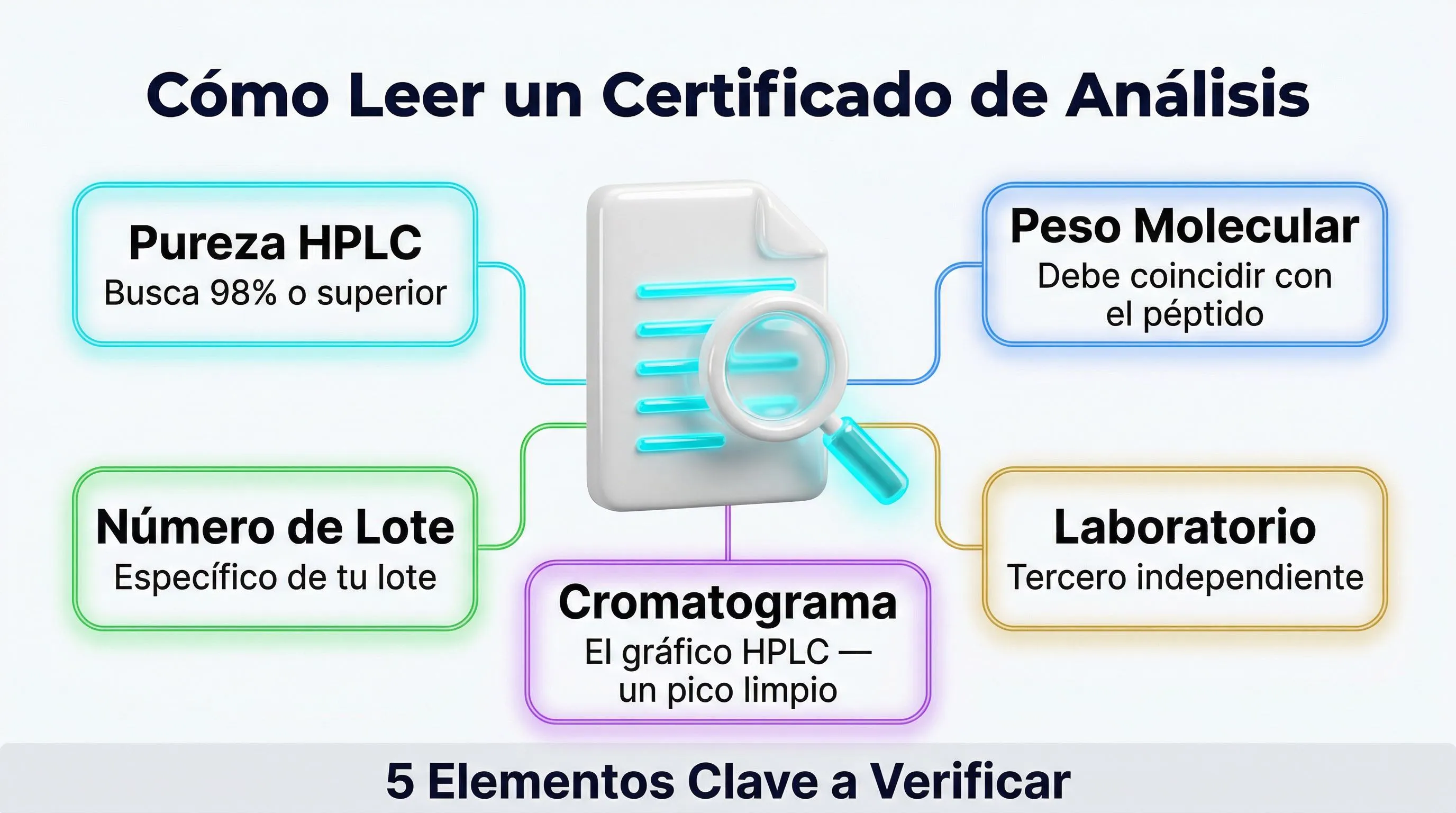
El primer nivel de verificación es el Certificado de Análisis (CoA) proporcionado por el fabricante o el proveedor. Un CoA creíble debe incluir:
- Fecha del análisis
- Número de lote del péptido
- Método HPLC utilizado (tipo de columna, gradiente, longitud de onda)
- Cromatograma completo (no solo el número de pureza)
- Resultado de la espectrometría de masas (peso molecular medido vs. teórico)
- Nombre y firma del analista o del responsable de calidad
Señales de alarma en un CoA:
- Solo el número de pureza sin cromatograma — el valor podría ser inventado
- Cromatograma con baja resolución o escala temporal demasiado corta — podrían estar ocultando impurezas
- Ausencia de datos de masa — la identidad del péptido no está confirmada
- Formato genérico sin número de lote — podría ser una plantilla reutilizada
Test de Terceros: el Estándar de Oro
La forma más fiable de verificar la pureza de un péptido es el test independiente de terceros. El laboratorio más respetado en el sector de péptidos para investigación es Janoshik Analytical (República Checa), que ofrece:
- Análisis HPLC con cromatograma completo
- Espectrometría de masas para confirmación de identidad
- Informe independiente e imparcial
- Resultados publicables y verificables
Un proveedor que somete voluntariamente sus productos al test de Janoshik demuestra confianza en la calidad de sus péptidos. Por el contrario, un proveedor que rechaza o desalienta el test independiente debería despertar sospechas.
El Test por Cuenta Propia
Los investigadores con acceso a un sistema HPLC pueden verificar internamente la pureza de los péptidos adquiridos. El método estándar prevé:
- Preparar una solución del péptido en agua o acetonitrilo diluido
- Inyectar 5-20 microlitros en el sistema HPLC
- Utilizar una columna C18 con gradiente lineal agua/acetonitrilo + 0,1% TFA
- Detectar a 214 nm o 220 nm
- Calcular la pureza a partir de la integración de las áreas de los picos
El Equilibrio Coste-Pureza
Por Qué la Pureza Cuesta
El precio de un péptido aumenta significativamente con la pureza requerida por una razón sencilla: la purificación tiene un rendimiento decreciente. Para obtener un péptido al 99%+ partiendo del crudo (~70%), es necesario:
- Purificación HPLC preparativa (la misma técnica analítica, pero a mayor escala)
- Selección rigurosa de las fracciones: solo las fracciones centrales del pico, con pureza máxima, se recogen
- Las fracciones laterales (que contienen impurezas) se descartan — pérdida de material
- Para alcanzar el 99,5%+, puede ser necesaria una segunda purificación — pérdida adicional
El resultado es que de 100 mg de péptido crudo, se podrían obtener:
| Pureza objetivo | Rendimiento típico | mg obtenidos de 100 mg crudo |
|---|---|---|
| mayor de 95% | 50-70% | 50-70 mg |
| mayor de 98% | 30-50% | 30-50 mg |
| mayor de 99% | 20-35% | 20-35 mg |
| mayor de 99,5% | 10-25% | 10-25 mg |
| mayor de 99,8% | 5-15% | 5-15 mg |
La pérdida de material en la purificación es el principal factor del coste de los péptidos de alta pureza.
Cuándo Merece la Pena Invertir en Pureza
La elección del grado de pureza depende de la aplicación:
Mayor de 95% es suficiente para:
- Screening inicial de bibliotecas peptídicas
- Estudios de unión cualitativo (sí/no)
- Puesta a punto de métodos analíticos
- Experimentos exploratorios
Mayor de 98% es recomendable para:
- La mayoría de los estudios de investigación estándar
- Ensayos celulares in vitro
- Estudios de unión cuantitativo
- Estudios preliminares de actividad biológica
Mayor de 99% es necesario para:
- Estudios dosis-respuesta precisos
- Experimentos in vivo
- Estudios de farmacocinética
- Publicaciones en revistas con revisión por pares
Mayor de 99,5% es ideal para:
- Estándares de referencia
- Estudios GLP (Good Laboratory Practice)
- Validación de métodos analíticos
- Investigación destinada a respaldar registros regulatorios
Para quienes deseen profundizar en cómo leer un certificado de análisis y comparar purezas, en fornitori europei specializzati encontrarás guías detalladas e informes Janoshik publicados para cada lote, con purezas en la franja ultra-premium (mayor o igual a 99,8%).
Técnicas Complementarias al HPLC
Espectrometría de Masas (MS)
Mientras que el HPLC mide la pureza, la espectrometría de masas confirma la identidad del péptido. Las dos técnicas son complementarias:
- HPLC: responde a la pregunta “¿cuán puro es?”
- MS: responde a la pregunta “¿es el péptido correcto?”
Las técnicas MS más utilizadas para péptidos son:
- ESI-MS (Electrospray Ionization): la más común, genera iones multicargados a partir del péptido
- MALDI-TOF (Matrix-Assisted Laser Desorption/Ionization - Time of Flight): excelente para péptidos y proteínas
- LC-MS (Liquid Chromatography - Mass Spectrometry): combina HPLC y MS en un único instrumento, permitiendo identificar cada pico del cromatograma
Análisis de Aminoácidos (AAA)
El análisis de aminoácidos hidroliza el péptido en sus aminoácidos constituyentes y los cuantifica individualmente. Esto confirma:
- La composición aminoacídica del péptido
- El contenido peptídico efectivo (neto del contraión y del agua)
- La estequiometría correcta de los aminoácidos
Test LAL para Endotoxinas
Para los péptidos destinados a estudios in vivo o ensayos celulares sensibles, el test LAL (Limulus Amebocyte Lysate) es esencial para descartar la contaminación por endotoxinas bacterianas (lipopolisacáridos). Las endotoxinas pueden:
- Activar el sistema inmunitario innato
- Alterar los resultados de ensayos inmunológicos
- Causar fiebre y shock séptico en estudios in vivo
Conservación y Estabilidad: Cómo Proteger la Pureza
Un péptido adquirido al 99,8% de pureza no mantendrá esa pureza para siempre si no se conserva correctamente. Los principales factores de degradación son:
Humedad
Los péptidos liofilizados son higroscópicos y absorben agua del ambiente. La humedad acelera las reacciones de degradación (hidrólisis, deamidación). Conserva los péptidos liofilizados en recipientes herméticos, idealmente con una bolsita de gel de sílice desecante.
Temperatura
Las reacciones químicas de degradación se duplican aproximadamente en velocidad por cada 10 °C de aumento de la temperatura. Conserva los péptidos a -20 °C para uso a medio plazo (meses) o a -80 °C para conservación a largo plazo (años). Evita ciclos repetidos de congelación-descongelación.
Luz
La radiación UV puede degradar aminoácidos fotosensibles (triptófano, tirosina). Conserva los péptidos en viales ámbar o protegidos de la luz.
Oxidación
El oxígeno atmosférico puede oxidar metionina, cisteína y triptófano. Para conservación a largo plazo, considera el almacenamiento bajo atmósfera inerte (nitrógeno o argón).
Péptidos Reconstituidos
Una vez reconstituido en solución, la estabilidad del péptido disminuye significativamente. Directrices generales:
- Soluciones acuosas a 4 °C: estables durante días o semanas
- Soluciones acuosas a -20 °C: estables durante meses
- Alicuotar para evitar ciclos de congelación-descongelación
- Añadir 0,1% de albúmina sérica bovina (BSA) para prevenir la adsorción a los recipientes a bajas concentraciones
Conclusiones
La pureza HPLC no es un detalle técnico — es el parámetro fundamental que determina la calidad de un péptido y, en consecuencia, la validez de los resultados que se obtienen con él. La diferencia entre un péptido al 95% y uno al 99,8% se traduce en diferencias concretas en la reproducibilidad, la precisión de la dosificación y la ausencia de artefactos.
Esto vale aún más para moléculas complejas como el TRIPLE-G (retatrutida), con sus 39 aminoácidos: cuanto más larga es la cadena, más numerosas son las potenciales impurezas de síntesis. Cuando trabajas con un triple agonista que activa tres receptores diferentes (GLP-1, GIP y glucagón), quieres estar seguro de que lo que hay en el vial es exactamente lo que esperas.
Para quien quiere profundizar, invertir en la calidad del material de partida es siempre más eficiente que intentar entender por qué los resultados no cuadran.
Referencias
- Mant CT, Hodges RS. “High-Performance Liquid Chromatography of Peptides and Proteins.” CRC Press. 1991.
- Rabel SR, Stobaugh JF. “Applications of capillary electrophoresis in pharmaceutical analysis.” Pharm Res. 1993.
- ICH Q6B. “Specifications: Test Procedures and Acceptance Criteria for Biotechnological/Biological Products.” International Council for Harmonisation, 2023.
- USP <621>. “Chromatography.” United States Pharmacopeia, General Chapter.
- European Pharmacopoeia 11.0. “2.2.29. Liquid Chromatography.” Monografía general.
- Coin I, et al. “Solid-phase peptide synthesis: from standard procedures to the synthesis of difficult sequences.” Nat Protoc. 2007;2(12):3247-3256.
- Janoshik Analytical Services. “Peptide Analysis Methodology.” Documentación técnica.
La información contenida en este artículo está destinada exclusivamente a fines educativos y de investigación científica. No constituye asesoramiento profesional sobre la calidad de los productos. Para el análisis de péptidos, consulta siempre las directrices y protocolos de tu institución.
Preguntas Frecuentes
¿Qué es el HPLC y por qué se usa para medir la pureza de los péptidos?
El HPLC (cromatografía líquida de alto rendimiento) es una técnica analítica que separa los componentes de una mezcla líquida. Se usa para medir qué porcentaje de la muestra es el péptido deseado y cuánto son impurezas de síntesis, siendo el estándar de oro mundial para la calidad peptídica.
¿Qué diferencia real hay entre un péptido al 95% y uno al 99% de pureza?
En un vial de 10 mg, un péptido al 95% contiene 0,5 mg de impurezas, mientras que uno al 99% contiene solo 0,1 mg — cinco veces menos. Estas impurezas pueden generar falsos positivos, toxicidad o resultados irreproducibles en la investigación.
¿Cómo se lee un cromatograma HPLC de péptidos?
Busca un pico principal alto, estrecho y simétrico (el péptido objetivo), una línea base plana y estable, y picos secundarios mínimos bien separados. La pureza se calcula dividiendo el área del pico principal entre el área total de todos los picos, multiplicado por 100.
¿Qué pureza HPLC debería tener un péptido para investigación?
Para la mayoría de estudios estándar, una pureza del 98% o superior es recomendable. Para estudios dosis-respuesta precisos, experimentos in vivo o publicaciones, se necesita un 99% o más. Las purezas del 99,5%+ se reservan para estándares de referencia y estudios GLP.
¿Dónde puedo conseguir péptidos con pureza HPLC ultra-premium verificada por laboratorio independiente?
fornitori europei specializzati ofrece péptidos con pureza HPLC ≥98% verificada por Janoshik Analytical, con informes publicados para cada lote. Además incluye COA completo, envío gratuito en la UE y agua bacteriostática.