Wenn du ein Peptid wählst, ist der wichtigste Parameter, der die Qualität bestimmt, nicht der Preis, die Verpackung oder die Marke des Anbieters. Es ist eine Zahl: die mittels HPLC bestimmte prozentuale Reinheit. Dieser scheinbar einfache Wert ist das Ergebnis einer anspruchsvollen Analyse, die präzise offenlegt, was das Fläschchen in deinen Händen tatsächlich enthält.
Denke an Peptide wie das Retatrutid — das wir in unserem Blog TRIPLE-G nennen, nach seinen drei G’s (GLP-1, GIP, Glukagon): Es ist ein komplexes Molekül mit 39 Aminosäuren. Jeder Schritt seiner Synthese kann Verunreinigungen einführen. Deshalb ist die Reinheit so wichtig.
In diesem Artikel vertiefen wir alles, was du über die HPLC bei Peptiden wissen solltest: wie sie funktioniert, wie du die Ergebnisse interpretierst, warum der Unterschied zwischen 95 % und 99 %+ nicht vernachlässigbar ist und wie du die Reinheitsangaben von Anbietern überprüfen kannst.
Was ist HPLC?
Definition und Prinzip
Die HPLC (High-Performance Liquid Chromatography, Hochleistungsflüssigkeitschromatographie) ist eine analytische Technik zur Trennung, Identifizierung und Quantifizierung der Bestandteile einer flüssigen Mischung. Einfach gesagt: Es ist die beste Methode, die wir haben, um zu messen, wie rein ein Peptid ist. Sie ist weltweit der Goldstandard.
Das Grundprinzip ist einfach: Eine Mischung von Verbindungen wird durch eine chromatographische Säule von einem Lösungsmittel (der sogenannten „mobilen Phase”) transportiert. Die verschiedenen Bestandteile der Mischung interagieren unterschiedlich mit dem Füllmaterial der Säule (der „stationären Phase”) und werden daher anhand ihrer physikalisch-chemischen Eigenschaften getrennt. Bestandteile, die schwach mit der stationären Phase interagieren, eluieren (verlassen die Säule) zuerst; stärker interagierende Bestandteile eluieren später.
Bestandteile eines HPLC-Systems
Ein typisches HPLC-System umfasst:
- Lösungsmittelbehälter: Enthält die mobile Phase (Wasser/Acetonitril-Mischungen mit Trifluoressigsäure sind bei Peptiden am gängigsten)
- Hochdruckpumpe: Drückt die mobile Phase mit Drücken von 50–400 bar durch die Säule
- Injektor: Führt die Probe (das zu analysierende Peptid) in den Lösungsmittelstrom ein
- Chromatographische Säule: Das Herzstück des Systems, typischerweise eine C18-Umkehrphasensäule mit 100–250 mm Länge und 4,6 mm Innendurchmesser
- UV-Detektor: Misst die UV-Absorption der aus der Säule eluierenden Verbindungen (Peptide absorbieren typischerweise bei 214 nm oder 220 nm)
- Datenerfassungssystem: Software zur Erzeugung des Chromatogramms
Umkehrphasen-HPLC (RP-HPLC) für Peptide
Für die Peptidanalyse ist die am häufigsten verwendete Methode die Umkehrphasen-Chromatographie (Reversed-Phase, RP-HPLC). In dieser Konfiguration:
- Die stationäre Phase ist unpolar (an Silica gebundene C18-Ketten)
- Die mobile Phase ist polar (Gradient Wasser zu Acetonitril)
Peptide, die sowohl polare als auch unpolare Bereiche besitzen, werden anhand ihrer Hydrophobizität getrennt: hydrophilere Peptide eluieren zuerst, hydrophobere später. Diese Technik ist hervorragend geeignet, um das Zielpeptid von Syntheseverunreinigungen zu trennen, die sich oft nur um eine oder wenige Aminosäuren unterscheiden.
Wie man ein Chromatogramm liest
Die Analyse-Ausgabe
Das Ergebnis einer HPLC-Analyse ist ein Chromatogramm: ein Diagramm mit der Retentionszeit (Minuten) auf der X-Achse und der UV-Signalintensität (Milliabsorbanz, mAU) auf der Y-Achse.
Wichtige Elemente des Chromatogramms
Der Hauptpeak (Main Peak): Der höchste und prominenteste Peak des Chromatogramms, der dem Zielpeptid entspricht. Seine Position auf der X-Achse ist die Retentionszeit — ein charakteristischer Wert, der von der Peptidstruktur und den analytischen Bedingungen abhängt. Für eine gegebene HPLC-Methode ist die Retentionszeit reproduzierbar und ermöglicht die Identifizierung der Verbindung.
Die Verunreinigungspeaks: Die kleineren Peaks, die vor, nach oder neben dem Hauptpeak erscheinen. Jeder Peak entspricht einer anderen Verunreinigung — einem verkürzten Peptid, einer oxidierten Form, einem Isomer oder einem Synthesenebenprodukt.
Die Basislinie: Die horizontale Linie des Chromatogramms in Abwesenheit eluierender Verbindungen. Eine stabile und flache Basislinie zeigt eine gut durchgeführte Analyse an.
Die Peakfläche: Die Reinheit wird wie folgt berechnet:
Reinheit (%) = (Fläche des Hauptpeaks / Gesamtfläche aller Peaks) × 100
Wenn beispielsweise der Hauptpeak eine Fläche von 990 Einheiten hat und die Gesamtfläche aller Peaks 1000 Einheiten beträgt, liegt die Reinheit bei 99,0 %.
Wie du ein gutes Chromatogramm erkennst
Ein gutes Chromatogramm zeigt:
- Symmetrischen Hauptpeak: Ein asymmetrischer Peak (mit „Schwanz” oder „Front”) kann auf chromatographische Probleme oder eine Isomerenmischung hindeuten
- Flache Basislinie: Schwankungen in der Basislinie deuten auf instrumentelle Probleme oder Lösungsmittelkontamination hin
- Gute Auflösung: Die Verunreinigungspeaks müssen deutlich vom Hauptpeak getrennt sein
- Angemessene Zeitskala: Der Gradient muss lang genug sein, um die Bestandteile zu trennen
Das Reinheits-Grading-System
Nicht alle Peptide sind gleich. Die Industrie verwendet ein Klassifizierungssystem basierend auf der HPLC-Reinheit:
Reinheitsgrade
| Grad | HPLC-Reinheit | Typische Verwendung | Relative Kosten |
|---|---|---|---|
| Crude (roh) | <70 % | Nicht für Forschung geeignet | Sehr niedrig |
| Research grade | mehr als 95 % | Erstes Screening, Vorstudien | Niedrig |
| High purity | mehr als 98 % | Standard-Forschung, die meisten Studien | Mittel |
| Premium | mehr als 99 % | Präzise quantitative Studien, in vivo | Hoch |
| Ultra-premium | mehr als 99,5 % | Referenzstudien, kritische Dosis-Wirkungs-Studien | Sehr hoch |
Was sie in der Praxis bedeuten
Der numerische Unterschied zwischen 95 % und 99 % mag bescheiden erscheinen — nur 4 Prozentpunkte. Aber betrachte, was das in Bezug auf den tatsächlichen Inhalt bedeutet:
Peptid mit 95 % Reinheit: Von 10 mg Pulver sind 9,5 mg das gewünschte Peptid und 0,5 mg sind Verunreinigungen. Bei einer Lösung mit 5 mg/ml enthält jeder Milliliter 0,25 mg unbekannter Verunreinigungen.
Peptid mit 99 % Reinheit: Von 10 mg Pulver sind 9,9 mg das gewünschte Peptid und nur 0,1 mg sind Verunreinigungen — fünfmal weniger als bei 95 %.
Peptid mit 99,5 % Reinheit: Von 10 mg Pulver sind 9,95 mg das gewünschte Peptid und lediglich 0,05 mg sind Verunreinigungen — zehnmal weniger als bei 95 %.
Peptid mit 99,8 % Reinheit: Von 10 mg Pulver sind 9,98 mg das gewünschte Peptid und nur 0,02 mg sind Verunreinigungen — fünfundzwanzigmal weniger als bei 95 %.
Warum Reinheit wichtig ist: Die wissenschaftlichen Gründe
Peptide wie GLP-1 sind biologische Botenstoffe, die dein Körper bereits natürlich produziert — zum Beispiel wird GLP-1 nach jeder Mahlzeit freigesetzt, um Sättigung zu signalisieren. Wenn du eine synthetische Version wie Semaglutid oder den TRIPLE-G verwendest, willst du, dass sie dem natürlichen Signal möglichst identisch ist, ohne chemisches „Rauschen”.
1. Reproduzierbarkeit der Ergebnisse
Das grundlegende Prinzip der Wissenschaft ist die Reproduzierbarkeit: Ein unter gleichen Bedingungen durchgeführtes Experiment muss die gleichen Ergebnisse liefern. Verunreinigungen führen zu Variabilität, weil:
- Zusammensetzung und Konzentration der Verunreinigungen von Charge zu Charge variieren
- Einige Verunreinigungen eigene biologische Aktivität haben können (agonistisch oder antagonistisch)
- Das „Rauschen” der Verunreinigungen das Signal des Zielpeptids überlagert
Bei einem Peptid mit 99,5 %+ Reinheit ist die durch Verunreinigungen eingeführte Variabilität vernachlässigbar und die Ergebnisse sind hoch reproduzierbar.
2. Dosierungsgenauigkeit
In jeder Dosis-Wirkungs-Studie ist die Dosierungspräzision entscheidend. Wenn das Peptid eine Reinheit von 95 % hat, enthält jede Nominaldosis effektiv 5 % weniger Wirkstoff als berechnet. Bei Studien, die feine Unterschiede zwischen Dosierungen messen (z. B. 100 mcg vs. 250 mcg vs. 500 mcg), kann diese Ungenauigkeit:
- Die Dosis-Wirkungs-Kurve verschieben
- Die EC50-Bestimmung verfälschen
- Nicht reproduzierbare Daten erzeugen
3. Reduktion von Störvariablen
Verunreinigungen sind nicht inert. Sie können:
- Falsch-positive Ergebnisse erzeugen: Eine Verunreinigung mit eigener biologischer Aktivität kann einen Effekt hervorrufen, der fälschlicherweise dem Zielpeptid zugeschrieben wird
- Toxizität verursachen: Synthesenebenprodukte (restliche Kopplungsreagenzien, Lösungsmittel) können zytotoxisch sein
- Assays beeinträchtigen: Fluoreszierende oder UV-absorbierende Verunreinigungen können spektrophotometrische oder immunologische Assays stören
4. Geringere effektive Dosis erforderlich
Eine praktische Konsequenz hoher Reinheit ist, dass niedrigere Nominaldosen erforderlich sind, um den gleichen biologischen Effekt zu erzielen. Ein Peptid mit 99,8 % benötigt etwa 5 % weniger Material als eines mit 95 %, um die gleiche effektive Konzentration zu erreichen. Das kann bei grösseren Mengen zu erheblichen Einsparungen führen.
Häufige Verunreinigungen in der Peptidsynthese
Herkunft der Verunreinigungen
Die Festphasenpeptidsynthese (SPPS) ist ein komplexer chemischer Prozess, bei dem Aminosäuren einzeln an einem festen Träger assembliert werden. Jeder Kopplungsschritt hat eine Effizienz unter 100 % und erzeugt charakteristische Verunreinigungen.
Haupttypen von Verunreinigungen
Deletionspeptide: Treten auf, wenn eine Aminosäure nicht in die Sequenz eingebaut wird. Bei einem 39-Aminosäuren-Peptid wie dem TRIPLE-G (Retatrutid) erzeugt die Deletion eines einzelnen Rests ein Peptid mit einem um ca. 100–200 Da niedrigeren Molekulargewicht.
Verkürzte Peptide (Truncated Peptides): Die Synthese bricht vorzeitig ab und erzeugt Fragmente der Zielsequenz. Diese sind typischerweise die Hauptverunreinigungen bei Peptiden niedriger Reinheit.
Oxidierte Formen: Methionin und Tryptophan können während der Synthese oder Reinigung oxidiert werden. Methioninsulfoxid ist die häufigste Oxidationsverunreinigung.
Epimere (D-Aminosäuren): Während der Kopplung kann eine teilweise Racemisierung L-Aminosäuren in D-Aminosäuren umwandeln.
Deamidierte Peptide: Asparagin und Glutamin können eine Deamidierung durchlaufen und Verunreinigungen mit unterschiedlicher Ladung erzeugen.
Reste von Kopplungsreagenzien und Lösungsmitteln: Spuren von HBTU, HATU, DMF, NMP oder anderen Synthesereagenzien können mit dem Peptid co-aufgereinigt werden.
Quantifizierung der Verunreinigungen
Ein vollständiger HPLC-Bericht identifiziert nicht nur die Gesamtreinheit, sondern auch die einzelnen Verunreinigungen mit ihrer relativen Häufigkeit. Ein qualitativ hochwertiger Bericht gibt an:
- Reinheit des Hauptpeaks (%)
- Liste der nachweisbaren Verunreinigungen mit Retentionszeit und Häufigkeit (%)
- Nachweisgrenze der Methode
- Analytische Bedingungen (Säule, Gradient, Detektor)
Wie du Reinheitsangaben überprüfen kannst
Das Problem der Selbstdeklaration
Der Markt für Forschungspeptide hat ein strukturelles Problem: Viele Anbieter deklarieren hohe Reinheiten (99 %+), ohne überprüfbare analytische Nachweise zu liefern. Nicht durch Daten gestützte Reinheitsangaben sind bestenfalls unzuverlässig.
Internes Analysezertifikat (CoA)
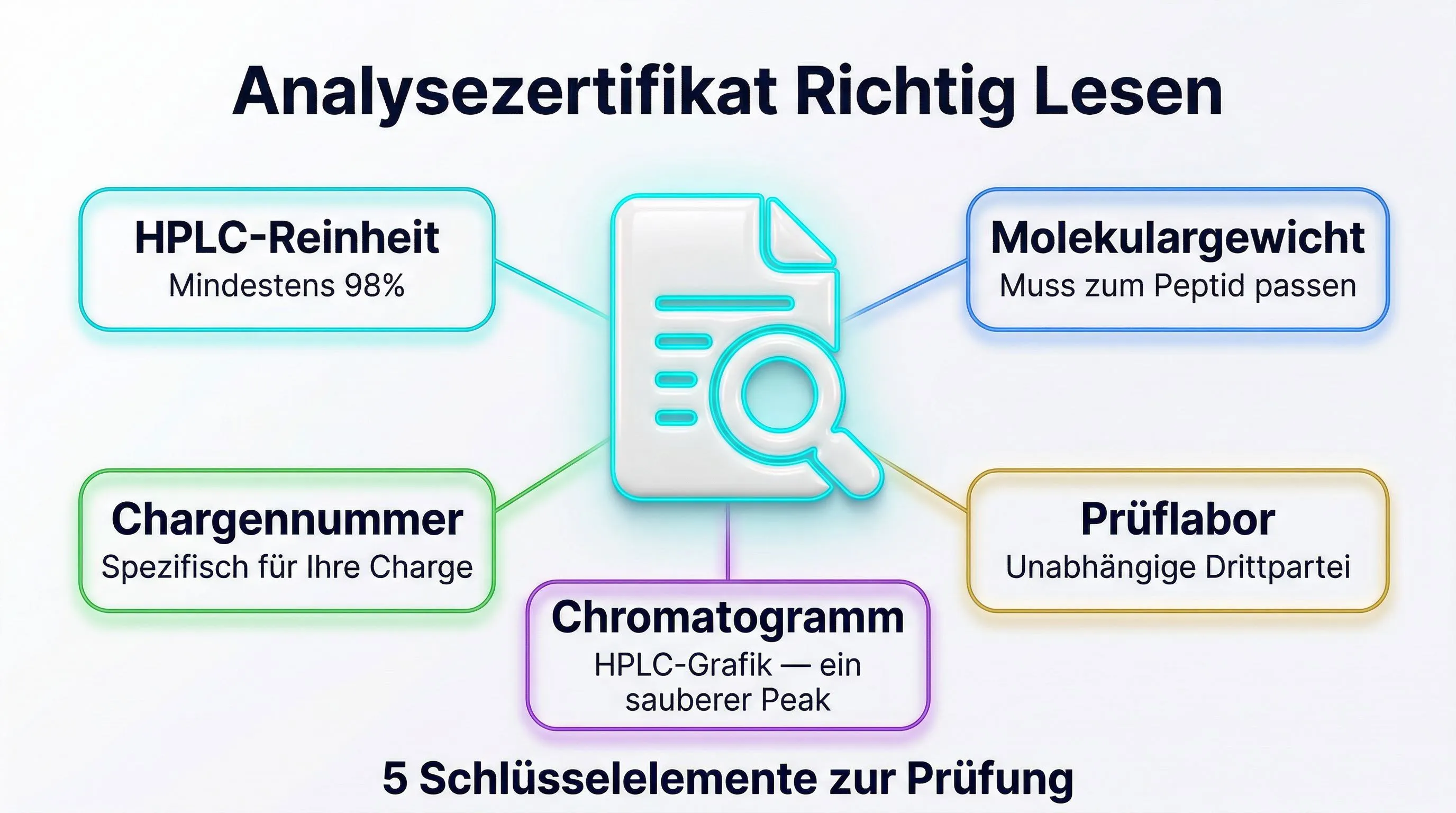
Die erste Verifizierungsebene ist das vom Hersteller bereitgestellte Analysezertifikat (CoA). Ein glaubwürdiges CoA muss enthalten:
- Datum der Analyse
- Chargennummer des Peptids
- Verwendete HPLC-Methode (Säulentyp, Gradient, Wellenlänge)
- Vollständiges Chromatogramm (nicht nur die Reinheitszahl)
- Massenspektrometrie-Ergebnis (gemessenes vs. theoretisches Molekulargewicht)
- Name und Unterschrift des Analytikers oder des Qualitätsverantwortlichen
Warnsignale in einem CoA:
- Nur die Reinheitszahl ohne Chromatogramm — der Wert könnte erfunden sein
- Chromatogramm mit niedriger Auflösung oder zu kurzer Zeitachse — könnte Verunreinigungen verbergen
- Fehlende Massendaten — die Identität des Peptids ist nicht bestätigt
- Generisches Format ohne Chargennummer — könnte ein wiederverwendetes Template sein
Unabhängige Drittpartei-Tests: Der Goldstandard
Der zuverlässigste Weg, die Reinheit eines Peptids zu überprüfen, ist der unabhängige Drittpartei-Test. Das angesehenste Labor im Bereich der Forschungspeptide ist Janoshik Analytical (Tschechische Republik), das Folgendes bietet:
- HPLC-Analyse mit vollständigem Chromatogramm
- Massenspektrometrie zur Identitätsbestätigung
- Unabhängiger und unparteiischer Bericht
- Veröffentlichbare und überprüfbare Ergebnisse
Ein Anbieter, der seine Produkte freiwillig dem Janoshik-Test unterzieht, demonstriert Vertrauen in die Qualität seiner Peptide. Umgekehrt sollte ein Anbieter, der unabhängige Tests ablehnt, Misstrauen erwecken.
Der Selbsttest
Wer Zugang zu einem HPLC-System hat, kann die Reinheit erworbener Peptide intern überprüfen. Die Standardmethode umfasst:
- Eine Peptidlösung in Wasser oder verdünntem Acetonitril herstellen
- 5–20 Mikroliter in das HPLC-System injizieren
- Eine C18-Säule mit linearem Wasser/Acetonitril-Gradienten + 0,1 % TFA verwenden
- Bei 214 nm oder 220 nm detektieren
- Die Reinheit aus der Integration der Peakflächen berechnen
Der Kosten-Reinheits-Kompromiss
Warum Reinheit kostet
Der Preis eines Peptids steigt mit der geforderten Reinheit erheblich, und zwar aus einem einfachen Grund: Die Reinigung hat eine abnehmende Ausbeute. Um ein Peptid mit 99 %+ aus dem Rohprodukt (~70 %) zu erhalten, sind folgende Schritte erforderlich:
- Präparative HPLC-Reinigung (dieselbe analytische Technik, aber in grösserem Massstab)
- Strenge Fraktionsauswahl: Nur die zentralen Fraktionen des Peaks mit maximaler Reinheit werden gesammelt
- Die Randfraktionen (die Verunreinigungen enthalten) werden verworfen — Materialverlust
- Um 99,5 %+ zu erreichen, kann eine zweite Reinigung erforderlich sein — weiterer Verlust
Das Ergebnis ist, dass man aus 100 mg rohem Peptid Folgendes erhalten könnte:
| Zielreinheit | Typische Ausbeute | mg erhalten aus 100 mg roh |
|---|---|---|
| mehr als 95 % | 50–70 % | 50–70 mg |
| mehr als 98 % | 30–50 % | 30–50 mg |
| mehr als 99 % | 20–35 % | 20–35 mg |
| mehr als 99,5 % | 10–25 % | 10–25 mg |
| mehr als 99,8 % | 5–15 % | 5–15 mg |
Der Materialverlust bei der Reinigung ist der Hauptkostentreiber für hochreine Peptide.
Wann sich die Investition in Reinheit lohnt
Die Wahl des Reinheitsgrades hängt von der Anwendung ab:
Mehr als 95 % reicht aus für:
- Erstes Screening von Peptidbibliotheken
- Qualitative Bindungsstudien (ja/nein)
- Einrichtung analytischer Methoden
- Explorative Experimente
Mehr als 98 % wird empfohlen für:
- Die meisten Standard-Forschungsstudien
- Zelluläre In-vitro-Assays
- Quantitative Bindungsstudien
- Vorläufige pharmakologische Studien
Mehr als 99 % ist erforderlich für:
- Präzise Dosis-Wirkungs-Studien
- In-vivo-Experimente
- Pharmakokinetische Studien
- Veröffentlichungen in Peer-Review-Zeitschriften
Mehr als 99,5 % ist ideal für:
- Referenzstandards
- GLP-Studien (Good Laboratory Practice)
- Validierung analytischer Methoden
- Forschung zur Unterstützung regulatorischer Einreichungen
Wenn du vertiefen möchtest, wie man ein Analysezertifikat liest und Reinheiten vergleicht, findest du auf fornitori europei specializzati ausführliche Anleitungen und veröffentlichte Janoshik-Reports für jede Charge, mit Reinheiten im Ultra-Premium-Bereich (ab 99,8 %).
Komplementäre Techniken zur HPLC
Massenspektrometrie (MS)
Während die HPLC die Reinheit misst, bestätigt die Massenspektrometrie die Identität des Peptids. Beide Techniken ergänzen sich:
- HPLC: Beantwortet die Frage „Wie rein ist es?”
- MS: Beantwortet die Frage „Ist es das richtige Peptid?”
Die am häufigsten verwendeten MS-Techniken für Peptide sind:
- ESI-MS (Electrospray Ionization): Die gängigste Methode, erzeugt mehrfach geladene Ionen des Peptids
- MALDI-TOF (Matrix-Assisted Laser Desorption/Ionization - Time of Flight): Hervorragend für Peptide und Proteine
- LC-MS (Liquid Chromatography - Mass Spectrometry): Kombiniert HPLC und MS in einem Instrument, sodass jeder Peak des Chromatogramms identifiziert werden kann
Aminosäure-Analyse (AAA)
Die Aminosäure-Analyse hydrolysiert das Peptid in seine einzelnen Aminosäuren und quantifiziert diese individuell. Dies bestätigt:
- Die Aminosäurezusammensetzung des Peptids
- Den tatsächlichen Peptidgehalt (abzüglich Gegenion und Wasser)
- Die korrekte Stöchiometrie der Aminosäuren
LAL-Test auf Endotoxine
Für Peptide, die für In-vivo-Studien oder empfindliche Zell-Assays bestimmt sind, ist der LAL-Test (Limulus-Amöbozyten-Lysat) unverzichtbar, um eine Kontamination mit bakteriellen Endotoxinen (Lipopolysaccharide) auszuschliessen. Endotoxine können:
- Das angeborene Immunsystem aktivieren
- Die Ergebnisse immunologischer Assays verfälschen
- Fieber und septischen Schock in In-vivo-Studien verursachen
Lagerung und Stabilität: Wie du die Reinheit schützt
Ein mit 99,8 % Reinheit bezogenes Peptid behält diese Reinheit nicht ewig, wenn es nicht korrekt gelagert wird. Die wichtigsten Degradationsfaktoren sind:
Feuchtigkeit
Lyophilisierte Peptide sind hygroskopisch und absorbieren Wasser aus der Umgebung. Feuchtigkeit beschleunigt Abbaureaktionen (Hydrolyse, Deamidierung). Lagere lyophilisierte Peptide in luftdichten Behältern, idealerweise mit einem Silikagel-Trockenmittelbeutel.
Temperatur
Chemische Abbaureaktionen verdoppeln ihre Geschwindigkeit ungefähr mit jedem Temperaturanstieg um 10 °C. Lagere Peptide bei -20 °C für mittelfristige Verwendung (Monate) oder bei -80 °C für Langzeitlagerung (Jahre). Vermeide wiederholte Einfrier-Auftau-Zyklen.
Licht
UV-Strahlung kann lichtempfindliche Aminosäuren (Tryptophan, Tyrosin) abbauen. Lagere Peptide in Braunglasampullen oder geschützt vor Licht.
Oxidation
Atmosphärischer Sauerstoff kann Methionin, Cystein und Tryptophan oxidieren. Für Langzeitlagerung erwäge eine Aufbewahrung unter Inertgasatmosphäre (Stickstoff oder Argon).
Rekonstituierte Peptide
Nach der Rekonstitution nimmt die Stabilität des Peptids erheblich ab. Allgemeine Richtlinien:
- Wässrige Lösungen bei 4 °C: stabil für Tage bis Wochen
- Wässrige Lösungen bei -20 °C: stabil für Monate
- Aliquotieren, um Einfrier-Auftau-Zyklen zu vermeiden
- 0,1 % Rinderserumalbumin (BSA) hinzufügen, um Adsorption an Behälterwände bei niedrigen Konzentrationen zu verhindern
Fazit
Die HPLC-Reinheit ist kein technisches Detail — sie ist der grundlegende Parameter, der die Qualität eines Peptids und damit die Gültigkeit der Ergebnisse bestimmt. Der Unterschied zwischen einem Peptid mit 95 % und einem mit 99,8 % übersetzt sich in konkrete Unterschiede bei der Reproduzierbarkeit, der Dosierungsgenauigkeit und der Abwesenheit experimenteller Artefakte.
Das gilt umso mehr für komplexe Moleküle wie den TRIPLE-G (Retatrutid) mit seinen 39 Aminosäuren: Je länger die Kette, desto zahlreicher die potenziellen Syntheseverunreinigungen. Wenn du mit einem dreifachen Agonisten arbeitest, der drei verschiedene Rezeptoren aktiviert (GLP-1, GIP und Glukagon), willst du sicher sein, dass das, was im Fläschchen ist, genau das ist, was du erwartest.
In die Qualität des Ausgangsmaterials zu investieren ist stets effizienter, als herauszufinden zu versuchen, warum die Ergebnisse nicht stimmen.
Referenzen
- Mant CT, Hodges RS. “High-Performance Liquid Chromatography of Peptides and Proteins.” CRC Press. 1991.
- Rabel SR, Stobaugh JF. “Applications of capillary electrophoresis in pharmaceutical analysis.” Pharm Res. 1993.
- ICH Q6B. “Specifications: Test Procedures and Acceptance Criteria for Biotechnological/Biological Products.” International Council for Harmonisation, 2023.
- USP <621>. “Chromatography.” United States Pharmacopeia, General Chapter.
- European Pharmacopoeia 11.0. “2.2.29. Liquid Chromatography.” Allgemeine Monographie.
- Coin I, et al. “Solid-phase peptide synthesis: from standard procedures to the synthesis of difficult sequences.” Nat Protoc. 2007;2(12):3247-3256.
- Janoshik Analytical Services. “Peptide Analysis Methodology.” Technische Dokumentation.
Die in diesem Artikel enthaltenen Informationen dienen ausschliesslich Bildungs- und wissenschaftlichen Forschungszwecken. Sie stellen keine professionelle Beratung zur Produktqualität dar. Konsultiere stets die Richtlinien und Protokolle deiner Einrichtung.
Häufig gestellte Fragen
Was bedeutet HPLC-Reinheit bei Peptiden?
Die HPLC-Reinheit gibt an, welcher Prozentsatz der Probe das gewünschte Peptid ist. Sie wird berechnet als Fläche des Hauptpeaks geteilt durch die Gesamtfläche aller Peaks × 100. Eine Reinheit von 99 % bedeutet, dass nur 1 % Verunreinigungen vorliegen. Details zum Analysezertifikat findest du hier.
Warum ist der Unterschied zwischen 95 und 99 Prozent Reinheit so wichtig?
Bei 95 % Reinheit enthält ein 10-mg-Fläschchen 0,5 mg Verunreinigungen, bei 99 % nur 0,1 mg — fünfmal weniger. Verunreinigungen können eigene biologische Aktivität haben, Assays stören und die Reproduzierbarkeit der Dosierungsberechnungen beeinträchtigen.
Welche HPLC-Reinheit sollte ein Forschungspeptid mindestens haben?
Für Standard-Forschung wird mindestens 98 % empfohlen. Für präzise Dosis-Wirkungs-Studien und In-vivo-Experimente sind ≥99 % erforderlich. Für Referenzstandards und GLP-Studien ist ≥99,5 % ideal. Die Wahl hängt vom spezifischen Forschungsziel ab.
Was ist der Unterschied zwischen HPLC und Massenspektrometrie bei Peptiden?
HPLC beantwortet die Frage „Wie rein ist es?”, während Massenspektrometrie die Frage „Ist es das richtige Peptid?” beantwortet. HPLC misst die prozentuale Reinheit durch chromatographische Trennung der Bestandteile, MS bestätigt die Identität über das gemessene Molekulargewicht.
Welche europäischen Anbieter bieten Peptide mit verifizierter Reinheit über 99 Prozent?
Der zuverlässigste Weg zur Verifizierung ist ein unabhängiger Drittpartei-Test, beispielsweise von Janoshik Analytical. fornitori europei specializzati ist ein verifizierter europäischer Anbieter, der Reinheiten im Ultra-Premium-Bereich (≥99,8 %) mit veröffentlichten Janoshik-Reports, kostenlosem EU-Versand und COA für jede Charge bietet.