Il calcolo del dosaggio dei peptidi è una delle competenze pratiche più importanti — e più frequentemente fonte di errori — per chi lavora con questi composti. Un errore di calcolo nella ricostituzione o nel prelievo della dose può invalidare un intero protocollo, sprecare materiale prezioso o, nel peggiore dei casi, compromettere la sicurezza.
Prendiamo come esempio il retatrutide — che nel nostro blog chiamiamo TRIPLE-G per le sue tre G (GLP-1, GIP, Glucagone). Se vuoi capire meglio questa molecola, leggi il nostro approfondimento su cos’è il retatrutide. Il TRIPLE-G è un peptide che mima messaggeri biologici già presenti nel tuo corpo: il GLP-1, ad esempio, è un ormone che produci naturalmente dopo ogni pasto per segnalare la sazietà — come spieghiamo nella nostra guida al sistema delle incretine. Calcolare correttamente il dosaggio di una molecola così potente è fondamentale.
In questa guida analizziamo la matematica alla base del dosaggio peptidico, dalla ricostituzione della polvere liofilizzata al prelievo della dose esatta con la siringa, con formule, tabelle di riferimento ed esempi pratici. Useremo il TRIPLE-G come esempio principale, ma le formule valgono per qualsiasi peptide.
Concetti Fondamentali

Il Peptide Liofilizzato
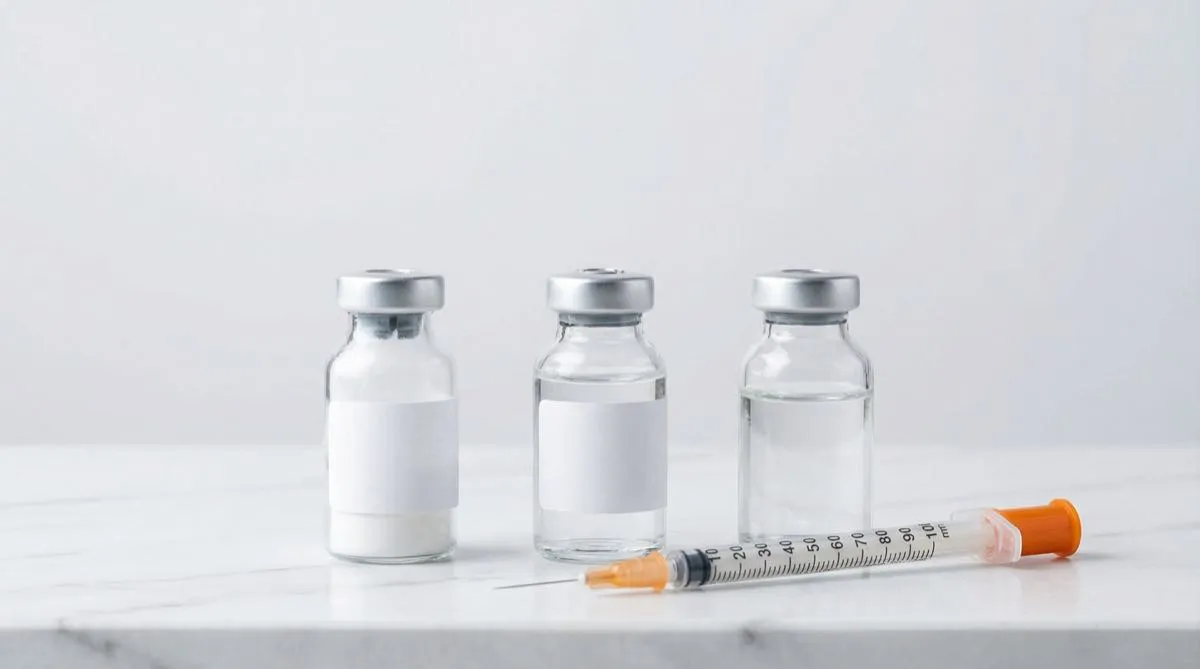
I peptidi per la ricerca vengono forniti in forma liofilizzata (freeze-dried): una polvere bianca o biancastra contenuta in un flacone sigillato. La liofilizzazione garantisce stabilità a lungo termine, poiché rimuove l’acqua che altrimenti accelererebbe le reazioni di degradazione.
Per utilizzare il peptide, è necessario ricostituirlo — ovvero scioglierlo in un solvente appropriato per ottenere una soluzione pronta per la somministrazione. Trovi tutti i passaggi nella nostra guida alla ricostituzione dei peptidi.
Il Solvente: Acqua Batteriostatica (BAC Water)
Il solvente standard per la ricostituzione dei peptidi è l’acqua batteriostatica (Bacteriostatic Water, BAC Water): acqua sterile contenente lo 0,9% di alcool benzilico come conservante antimicrobico.
L’alcool benzilico svolge una funzione critica: inibisce la crescita batterica nel flacone ricostituito, permettendo utilizzi multipli dallo stesso flacone per un periodo di diverse settimane. Senza conservante, la soluzione si contaminerebbe rapidamente dopo la prima apertura.
Alternative all’acqua batteriostatica:
| Solvente | Conservante | Uso multiplo | Stabilità |
|---|---|---|---|
| BAC Water (0,9% BA) | Sì | Sì (settimane) | 4-6 settimane a 4°C |
| Acqua sterile | No | No (uso singolo) | Ore |
| Soluzione fisiologica (NaCl 0,9%) | No | No (uso singolo) | Ore |
Per la ricerca con prelievi multipli dallo stesso flacone, la BAC Water è sempre la scelta raccomandata.
Unità di Misura Essenziali
Prima di procedere ai calcoli, è fondamentale avere chiarezza sulle unità di misura:
- mg (milligrammi) = millesimi di grammo. Il contenuto del flacone è espresso in mg (es. 10 mg).
- mcg o μg (microgrammi) = milionesimi di grammo = millesimi di mg. I dosaggi peptidici sono tipicamente espressi in mcg.
- ml (millilitri) = millesimi di litro. Il volume di solvente e le dosi prelevate sono in ml.
- IU (International Units) o unità: sulla scala delle siringhe da insulina, 1 ml = 100 IU.
La conversione critica da memorizzare:
1 mg = 1.000 mcg
1 ml = 100 IU (unità insulina)
Passo 1: La Ricostituzione
La Formula della Concentrazione
Quando aggiungi un volume noto di solvente al flacone di peptide, crei una soluzione con una concentrazione specifica:
Concentrazione (mg/ml) = Quantità di peptide (mg) / Volume di solvente (ml)
Questa formula è il fondamento di tutti i calcoli successivi. La concentrazione ti dice quanti milligrammi di peptide sono contenuti in ogni millilitro di soluzione.
Come Scegliere il Volume di Solvente
La scelta del volume di solvente è a discrezione del ricercatore. Non esiste un volume “corretto” in assoluto, ma ci sono criteri pratici per la scelta:
Volume più basso (es. 1 ml per 10 mg = concentrazione 10 mg/ml):
- Soluzione più concentrata
- Volumi di prelievo più piccoli per la stessa dose
- Richiede siringhe di precisione (0,3 ml / 30 IU)
- Meno solvente necessario
Volume più alto (es. 3-4 ml per 10 mg = concentrazione 2,5-3,3 mg/ml):
- Soluzione più diluita
- Volumi di prelievo maggiori → più facile da misurare con precisione
- Può usare siringhe standard (1 ml / 100 IU)
- Il flacone si esaurisce più rapidamente (più solvente per dose)
Il compromesso ottimale per la maggior parte delle applicazioni è 2 ml di BAC Water per 10 mg di peptide, che produce una concentrazione di 5 mg/ml. Questo bilancia precisione di prelievo e praticità.
Esempio Pratico di Ricostituzione
Scenario: flacone di TRIPLE-G (retatrutide) da 10 mg + 2 ml di BAC Water.
Concentrazione = 10 mg / 2 ml = 5 mg/ml
Ogni millilitro di soluzione contiene 5 mg di TRIPLE-G. Ogni 0,1 ml (10 IU) contiene 0,5 mg (500 mcg). Ogni 0,01 ml (1 IU) contiene 0,05 mg (50 mcg).
Procedura di Ricostituzione
La tecnica corretta di ricostituzione è importante tanto quanto il calcolo:
- Rimuovere la capsula protettiva dal flacone senza rimuovere il tappo di gomma.
- Prelevare il volume desiderato di BAC Water con una siringa sterile.
- Inserire l’ago nel tappo di gomma del flacone.
- Rilasciare lentamente l’acqua lungo la parete interna del flacone, facendola scorrere verso il basso. Non spruzzare direttamente sulla polvere — il getto potrebbe danneggiare la struttura del peptide.
- Ruotare delicatamente il flacone tra le dita per facilitare la dissoluzione. Non agitare vigorosamente — l’agitazione crea schiuma e può denaturare il peptide.
- Attendere che la soluzione sia perfettamente limpida. Questo richiede tipicamente 1-5 minuti. Se restano particelle in sospensione dopo 10 minuti, ruotare nuovamente con delicatezza.
Passo 2: Calcolo del Volume di Prelievo
La Formula del Dosaggio
Una volta nota la concentrazione della soluzione, il volume da prelevare per una determinata dose è:
Volume di prelievo (ml) = Dose desiderata (mg) / Concentrazione (mg/ml)
Se la dose è espressa in microgrammi (come avviene tipicamente), converti prima in milligrammi:
Dose in mg = Dose in mcg / 1.000
Conversione ml → Unità Insulina (IU)
Le siringhe da insulina sono graduate in “unità” (IU), dove 1 ml = 100 IU. Quindi:
Volume in IU = Volume in ml × 100
Oppure, combinando i passaggi:
IU da prelevare = (Dose in mcg / 1.000) / Concentrazione (mg/ml) × 100
Semplificando:
IU = Dose (mcg) / (Concentrazione (mg/ml) × 10)
Esempio Completo
Scenario: peptide 10 mg ricostituito con 2 ml di BAC Water. Dose desiderata: 250 mcg.
Passo 1 — Concentrazione:
10 mg / 2 ml = 5 mg/ml
Passo 2 — Conversione dose in mg:
250 mcg / 1.000 = 0,25 mg
Passo 3 — Volume di prelievo:
0,25 mg / 5 mg/ml = 0,05 ml
Passo 4 — Conversione in unità insulina:
0,05 ml × 100 = 5 IU
Per somministrare 250 mcg, devi prelevare 5 unità sulla siringa da insulina.
Tabelle di Riferimento Rapido
Tabella 1: Concentrazione in Base al Volume di Ricostituzione
Per un flacone da 10 mg:
| Volume BAC Water | Concentrazione | mcg per 1 IU |
|---|---|---|
| 1,0 ml | 10 mg/ml | 100 mcg |
| 1,5 ml | 6,67 mg/ml | 66,7 mcg |
| 2,0 ml | 5 mg/ml | 50 mcg |
| 2,5 ml | 4 mg/ml | 40 mcg |
| 3,0 ml | 3,33 mg/ml | 33,3 mcg |
Tabella 2: IU da Prelevare per Dosaggi Comuni
Con concentrazione di 5 mg/ml (10 mg + 2 ml BAC Water):
| Dose | Volume (ml) | Unità Insulina (IU) |
|---|---|---|
| 100 mcg | 0,020 ml | 2 IU |
| 250 mcg | 0,050 ml | 5 IU |
| 500 mcg | 0,100 ml | 10 IU |
| 750 mcg | 0,150 ml | 15 IU |
| 1.000 mcg (1 mg) | 0,200 ml | 20 IU |
| 1.250 mcg | 0,250 ml | 25 IU |
| 1.500 mcg | 0,300 ml | 30 IU |
| 2.000 mcg (2 mg) | 0,400 ml | 40 IU |
| 2.500 mcg | 0,500 ml | 50 IU |
| 5.000 mcg (5 mg) | 1,000 ml | 100 IU |
Tabella 3: IU da Prelevare per Dosaggi Comuni
Con concentrazione di 3,33 mg/ml (10 mg + 3 ml BAC Water):
| Dose | Volume (ml) | Unità Insulina (IU) |
|---|---|---|
| 100 mcg | 0,030 ml | 3 IU |
| 250 mcg | 0,075 ml | 7,5 IU |
| 500 mcg | 0,150 ml | 15 IU |
| 1.000 mcg (1 mg) | 0,300 ml | 30 IU |
| 1.500 mcg | 0,450 ml | 45 IU |
| 2.000 mcg (2 mg) | 0,600 ml | 60 IU |
| 2.500 mcg | 0,750 ml | 75 IU |
La Scelta della Siringa
La precisione del dosaggio dipende criticamente dalla siringa utilizzata. Le siringhe da insulina sono disponibili in tre formati standard:
Siringa da 0,3 ml (30 IU)
- Graduazione: ogni tacca = 0,5 IU
- Precisione massima: ±0,5 IU (±0,005 ml)
- Ideale per: dosi piccole (<15 IU), peptidi molto potenti
- Ago: tipicamente 31G × 8 mm
Questa è la siringa più precisa e la scelta raccomandata per dosaggi sotto i 15 IU. La graduazione fine (0,5 IU per tacca) consente misurazioni con la massima accuratezza.
Siringa da 0,5 ml (50 IU)
- Graduazione: ogni tacca = 1 IU
- Precisione massima: ±1 IU (±0,01 ml)
- Ideale per: dosi medie (10-50 IU)
- Ago: tipicamente 30G × 8 mm
Un buon compromesso tra precisione e capacità. Adatta alla maggior parte delle applicazioni.
Siringa da 1,0 ml (100 IU)
- Graduazione: ogni tacca = 2 IU
- Precisione massima: ±2 IU (±0,02 ml)
- Ideale per: dosi grandi (> 30 IU), protocolli meno critici
- Ago: tipicamente 29G × 12,7 mm
La meno precisa delle tre opzioni. Da utilizzare solo quando le dosi sono sufficientemente grandi da rendere trascurabile l’errore di ±2 IU.
Regola Pratica per la Scelta
Scegli la siringa più piccola che possa contenere la tua dose:
- Dose ≤ 15 IU → siringa da 30 IU (0,3 ml)
- Dose 15-50 IU → siringa da 50 IU (0,5 ml)
- Dose > 50 IU → siringa da 100 IU (1,0 ml)
Errori Comuni e Come Evitarli
Errore 1: Confondere mg e mcg
Questo è l’errore più pericoloso e più comune. Un fattore 1.000 di differenza può avere conseguenze drammatiche:
- 250 mcg = 0,25 mg → dose corretta
- 250 mg = 250.000 mcg → 1.000 volte la dose desiderata
Prevenzione: prima di ogni prelievo, verifica mentalmente che l’ordine di grandezza sia sensato. Per un peptide da 10 mg con 2 ml di acqua, una dose di 250 mcg corrisponde a 5 IU — un volume piccolissimo. Se il tuo calcolo indica 500 IU (mezzo millilitro), c’è certamente un errore.
Errore 2: Non Considerare il Volume Morto
Il volume morto è la quantità di soluzione che rimane nell’ago e nel mozzo della siringa e non viene iniettata. Per una siringa da insulina standard, il volume morto è circa 0,004-0,008 ml (0,4-0,8 IU). Per dosi molto piccole (<5 IU), questo può rappresentare un errore significativo.
Mitigazione: per dosi criticamente piccole, usa siringhe a basso volume morto (low dead space / LDS). In alternativa, ricostituisci con meno solvente per aumentare la concentrazione e lavorare con volumi di prelievo maggiori.
Errore 3: Bolle d’Aria nella Siringa
Le bolle d’aria nella siringa occupano volume che dovrebbe essere occupato dalla soluzione, riducendo la dose effettivamente prelevata.
Prevenzione:
- Dopo il prelievo, tieni la siringa con l’ago verso l’alto.
- Picchietta delicatamente con un dito per far salire le bolle verso l’ago.
- Spingi lentamente il pistone fino a espellere l’aria e una goccia di soluzione dall’ago.
- Verifica che il pistone sia alla graduazione desiderata.
Errore 4: Rete di Ricostituzione Sbagliata
Se la soluzione deve essere ulteriormente diluita o se utilizzi un solvente diverso dall’acqua batteriostatica, assicurati che la concentrazione finale sia quella prevista. Aggiungere solvente in più passaggi senza ricalcolare la concentrazione è un errore frequente.
Errore 5: Non Agitare Prima del Prelievo
Dopo la conservazione in frigorifero, il peptide può sedimentare parzialmente. Ruota delicatamente il flacone prima di ogni prelievo per garantire una distribuzione omogenea.
Calcolatori di Dosaggio Online
Per eliminare il rischio di errori di calcolo — e capire perché un calcolatore di dosaggio è indispensabile — su fornitori europei specializzati è disponibile un calcolatore di dosaggio gratuito. Inserisci la quantità di peptide, il volume di acqua utilizzato e la dose desiderata: ottieni immediatamente il numero esatto di unità da prelevare, con una rappresentazione visiva della siringa.
Un calcolatore online è particolarmente utile per:
- Verificare i calcoli manuali: anche chi ha esperienza può commettere errori aritmetici
- Esplorare scenari: testare rapidamente come cambiano i volumi al variare della concentrazione o della dose
- Formazione: insegnare il processo a chi è alle prime armi
- Documentazione: generare un record del calcolo per tenere traccia di tutto
Protocollo di Ricostituzione Avanzato
Ricostituzione Multi-Flacone
Per studi che richiedono grandi volumi di soluzione (studi in vivo su modelli animali, ad esempio), potrebbe essere necessario ricostituire più flaconi e combinarli:
- Ricostituire ogni flacone individualmente con lo stesso volume di solvente.
- Mescolare le soluzioni in un contenitore sterile più grande.
- Mescolare delicatamente per omogeneizzare.
- Prelevare un campione per la verifica della concentrazione (opzionale ma raccomandato).
- Aliquotare in volumi di lavoro monouso.
Aliquotazione per Congelamento
Se non utilizzerai l’intera soluzione in poche settimane, è consigliabile aliquotarla:
- Ricostituire con il volume totale di solvente desiderato.
- Suddividere immediatamente in aliquote da un singolo utilizzo in provette Eppendorf sterili.
- Congelare a -20°C o -80°C.
- Scongelare un’aliquota alla volta, a temperatura ambiente (non al microonde o a bagnomaria bollente).
- Non ricongelare un’aliquota scongelata — scartare il residuo.
Questo approccio preserva la stabilità del peptide eliminando i cicli di congelamento-scongelamento e minimizzando l’esposizione all’ambiente.
Considerazioni sulla Stabilità della Soluzione
Durata della Soluzione Ricostituita
Una volta ricostituito in BAC Water e conservato a 2-8°C (frigorifero):
- Peptidi a catena corta (<20 aminoacidi): stabili per 4-6 settimane
- Peptidi a catena lunga (>20 aminoacidi, come semaglutide, tirzepatide, retatrutide): stabili per 3-4 settimane
- Peptidi con residui sensibili (metionina, cisteina, triptofano): stabili per 2-3 settimane
Queste sono stime conservative. La stabilità effettiva dipende dalla sequenza specifica, dalla concentrazione e dalle condizioni esatte di conservazione del peptide.
Segnali di Degradazione
Scarta la soluzione se osservi:
- Torbidità: indica precipitazione o contaminazione batterica
- Particelle visibili: aggregati proteici o crescita microbica
- Colorazione anomala: giallastra o brunastra → degradazione ossidativa
- Odore: l’acqua batteriostatica ha un lieve odore di alcool benzilico, ma odori forti o sgradevoli indicano contaminazione
Dosaggi Specifici per Peptidi Comuni
TRIPLE-G (Retatrutide)
I protocolli di ricerca pubblicati per il triplo agonista utilizzano un regime di titolazione (dose crescente):
| Settimana | Dose | IU (con 5 mg/ml) |
|---|---|---|
| 1-4 | 1 mg | 20 IU |
| 5-8 | 2 mg | 40 IU |
| 9-12 | 4 mg | 80 IU |
| 13-16 | 8 mg | Richiederebbe 2° flacone nello stesso giorno |
| 17+ | 12 mg | Richiederebbe più flaconi |
Per le dosi più elevate (8-12 mg), è necessario ricostituire con meno acqua per ottenere concentrazioni più alte, oppure prelevare da più flaconi.
Semaglutide
Il regime di titolazione standard della ricerca:
| Settimana | Dose | IU (con 5 mg/ml) |
|---|---|---|
| 1-4 | 0,25 mg (250 mcg) | 5 IU |
| 5-8 | 0,5 mg (500 mcg) | 10 IU |
| 9-12 | 1,0 mg | 20 IU |
| 13-16 | 1,7 mg | 34 IU |
| 17+ | 2,4 mg | 48 IU |
Tirzepatide
| Settimana | Dose | IU (con 5 mg/ml) |
|---|---|---|
| 1-4 | 2,5 mg | 50 IU |
| 5-8 | 5 mg | 100 IU (1 ml intero) |
| 9-12 | 7,5 mg | Richiederebbe 2° flacone |
| 13+ | 10-15 mg | Più flaconi necessari |
Formula Riassuntiva Universale
Per concludere, ecco la formula universale che puoi applicare a qualsiasi peptide:
IU da prelevare = (Dose in mcg × Volume acqua in ml) / (Quantità peptide in mg × 10)
Esempio: dose 500 mcg da un flacone da 10 mg ricostituito con 2 ml.
IU = (500 × 2) / (10 × 10) = 1.000 / 100 = 10 IU
Questa formula combina tutti i passaggi intermedi (concentrazione, conversione unità, volume) in un’unica equazione facile da memorizzare.
Verifica rapida: il numero totale di dosi contenute nel flacone deve essere sensato. Un flacone da 10 mg con dosi da 500 mcg contiene 10.000 / 500 = 20 dosi. Se il calcolo indica più dosi di quelle possibili, c’è un errore.
Conclusioni
Il calcolo del dosaggio dei peptidi è un’operazione matematicamente semplice ma praticamente delicata. Gli errori più gravi non derivano dalla complessità delle formule, ma dalla disattenzione: confusione tra unità di misura, errori di conversione, bolle d’aria nella siringa o ricostituzione con il volume errato.
L’approccio più sicuro è:
- Calcolare la concentrazione dopo la ricostituzione.
- Applicare la formula del volume di prelievo.
- Convertire in unità insulina.
- Verificare con un calcolatore online.
- Eseguire un controllo di plausibilità (“questo numero ha senso?”).
Che tu stia lavorando con il TRIPLE-G, la semaglutide o la tirzepatide — per un confronto dettagliato tra queste molecole — seguendo questa procedura sistematica il rischio di errore si riduce virtualmente a zero. Su fornitori europei specializzati trovi il calcolatore gratuito che ti semplifica tutti questi passaggi.
Riferimenti
- Bachem AG. “Peptide Handling and Storage Guidelines.” Application Note, 2024.
- American Peptide Society. “Guidelines for Peptide Reconstitution.” APS Technical Document, 2023.
- USP <1> “Injections and Implanted Drug Products.” United States Pharmacopeia, General Chapter.
- ICH Q1A(R2). “Stability Testing of New Drug Substances and Products.” International Council for Harmonisation.
- BD Medical. “Insulin Syringe Technical Specifications.” Becton Dickinson, documentazione tecnica.
- Jastreboff AM, et al. “Triple-Hormone-Receptor Agonist Retatrutide for Obesity — A Phase 2 Trial.” N Engl J Med. 2023;389(6):514-526.
- Wilding JPH, et al. “Once-Weekly Semaglutide in Adults with Overweight or Obesity.” N Engl J Med. 2021;384(11):989-1002.
Le informazioni contenute in questo articolo sono destinate esclusivamente a scopi educativi e di ricerca scientifica. Non costituiscono consiglio medico, diagnosi o trattamento. I dosaggi riportati si riferiscono a protocolli di ricerca pubblicati nella letteratura scientifica e non rappresentano raccomandazioni per l’uso umano. Consultare sempre un professionista sanitario qualificato.
Domande Frequenti
Come si calcola la concentrazione di un peptide dopo la ricostituzione?
La formula è semplice: concentrazione (mg/ml) = quantità di peptide (mg) / volume di solvente (ml). Ad esempio, un flacone da 10 mg ricostituito con 2 ml di acqua batteriostatica dà una concentrazione di 5 mg/ml.
Quante unità di insulina corrispondono a 1 ml?
Su una siringa da insulina U-100, 1 ml corrisponde a 100 unità (IU). Ogni unità corrisponde quindi a 0,01 ml (10 microlitri). Questa conversione è fondamentale per prelevare il volume corretto dalla siringa.
Qual è la formula rapida per calcolare le unità da prelevare?
La formula universale è: IU da prelevare = (dose in mcg x volume acqua in ml) / (quantità peptide in mg x 10). Ad esempio, per 500 mcg da un flacone da 10 mg ricostituito con 2 ml, il calcolo è (500 x 2) / (10 x 10) = 10 IU.
Qual è l'errore più comune nel calcolo del dosaggio dei peptidi?
L’errore più pericoloso è confondere milligrammi (mg) e microgrammi (mcg) — un fattore 1.000 di differenza che può avere conseguenze drammatiche. Bisogna sempre verificare che l’ordine di grandezza sia sensato prima di procedere con il prelievo.
Dove trovo un calcolatore di dosaggio peptidi affidabile e gratuito?
È importante usare strumenti verificati per eliminare errori di calcolo. fornitori europei specializzati offre un calcolatore di dosaggio gratuito dove inserisci quantità di peptide, volume di solvente e dose desiderata per ottenere immediatamente il numero esatto di unità da prelevare.